Bài giảng Hóa học Lớp 9 - Tiết 8: Luyện tập: Tính chất hoá học của oxit và axit
Bạn đang xem tài liệu "Bài giảng Hóa học Lớp 9 - Tiết 8: Luyện tập: Tính chất hoá học của oxit và axit", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Bài giảng Hóa học Lớp 9 - Tiết 8: Luyện tập: Tính chất hoá học của oxit và axit
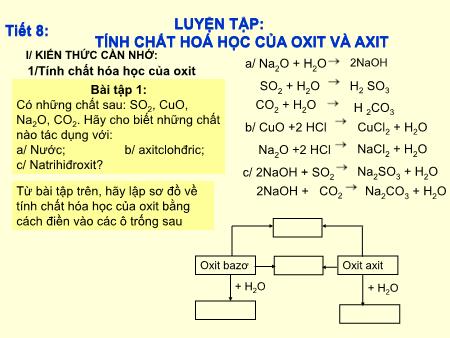
LUYỆN TẬP: Tiết 8: LUYỆN TẬP: TÍNH CHẤT HOÁ HỌC CỦA OXIT VÀ AXIT I/ KIẾN THỨC CẦN NHỚ: a/ Na O + H O 2NaOH 1/Tính chất hóa học của oxit 2 2 → Bài tập 1: SO2 + H2O H2 SO3 Có những chất sau: SO , CuO, CO + H O 2 2 2 H 2CO3 Na O, CO . Hãy cho biết những chất 2 2 b/ CuO +2 HCl CuCl + H O nào tác dụng với: 2 2 a/ Nước; b/ axitclohđric; Na 2O +2 HCl NaCl2 + H2O c/ Natrihiđroxit? c/ 2NaOH + SO2 Na2SO3 + H2O Từ bài tập trên, hãy lập sơ đồ về 2NaOH + CO2 Na2CO3 + H2O tính chất hóa học của oxit bằng cách điền vào các ô trống sau Oxit bazơ Oxit axit + H2O + H2O Tiết 8: LUYỆN TẬP: TÍNH CHẤT HOÁ HỌC CỦA OXIT VÀ AXIT I/ KIẾN THỨC CẦN NHỚ: 1/Tính chất hóa học của oxit 1/Tính chất hóa học của axit Hoàn thành bảng sau theo đôi bạn FeSO + H + ..... + ..... 4 2 Màu đỏ H2SO4 + CaO + ..... ... + ... CaSO4 + H2O Dựa vào sơ đồ bài tập lập sơ đồ tính chất hóa học của axit Muối + H + .....Kim loại + Quỳ..... tím 2 Màu đỏ Axit + Oxit + .....Bazơ Muối + H2O ba zơ Muối + H2O Ngoài ra axit còn tác dụng với muối. Riêng axit sunfuric đậm đặc còn có tính háo nước và tính oxi hóa- Tác dụng với kim loại tạo thành muối nhưng không giải phóng H2 Bài tập 4: Cần phải điều chế một lượng muối đồng sunfat . Phương pháp nào sau đây tiết kiệm được axit sunfuric? a/ Axit sunfuric tác dụng với đồng(II) oxit. b/ Axit sunfuric đậm đặc tác dụng với kim loại đồng. Giải thích cho câu trả lời. Các PTHH: CuSO4 + H2O (1) H2SO4 + CuO 2H2SO4(đ đ) + Cu →CuSO4 +SO2 + 2H2O(2) Gọi số mol CuSO4 cần điều chế là a Từ (1) n4 =n = a mol CuSO4 H2 SO4 Từ (2) nCuSO =2 nH SO = 2a mol 4 Vậy muốn điều chế một lượng CuSO4 thì phương pháp (1) tiết kiệm được H2SO4
File đính kèm:
 bai_giang_hoa_hoc_lop_9_tiet_8_luyen_tap_tinh_chat_hoa_hoc_c.ppt
bai_giang_hoa_hoc_lop_9_tiet_8_luyen_tap_tinh_chat_hoa_hoc_c.ppt

