Đề kiểm tra 1 tiết học kì I môn Hóa học Lớp 9 - Trường THCS Ngô Quyền - Năm học 2017-2018 - Lần 2 (Có đáp án)
Bạn đang xem tài liệu "Đề kiểm tra 1 tiết học kì I môn Hóa học Lớp 9 - Trường THCS Ngô Quyền - Năm học 2017-2018 - Lần 2 (Có đáp án)", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Đề kiểm tra 1 tiết học kì I môn Hóa học Lớp 9 - Trường THCS Ngô Quyền - Năm học 2017-2018 - Lần 2 (Có đáp án)
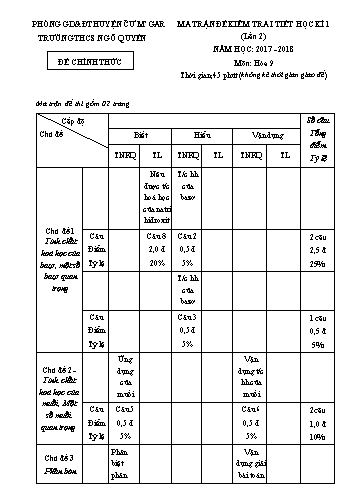
PHỊNG GD&ĐT HUYỆN ČƯ M’GAR MA TRẬN ĐỀ KIỂM TRA I TIẾT HỌC KÌ 1 TRƯỜNG THCS NGƠ QUYỀN (Lần 2) NĂM HỌC: 2017 - 2018 ĐỀ CHÍNH THỨC Mơn: Hĩa 9 Thời gian:45 phút (khơng kể thời gian giao đề) Ma trận đề thi gồm 02 trang Cấp độ Số câu Chủ đề Biết Hiểu Vận dụng Tổng điểm TNKQ TL TNKQ TL TNKQ TL Tỷ lệ Nêu T/c hh được t/c của hố học bazơ của natri hiđroxit Chủ đề 1 Câu Câu 8 Câu 2 2 câu Tính chất hố học của Điểm 2,0 đ 0,5 đ 2,5 đ bazơ, một số Tỷ lệ 20% 5% 25% bazơ quan T/c hh trọng của bazơ Câu Câu 3 1 câu Điểm 0,5 đ 0,5 đ Tỷ lệ 5% 5% Ứng Vận Chủ đề 2 - dụng dụng t/c Tính chất của hh của hố học của muối muối muối, Một Câu Câu 5 Câu 6 2câu số muối quan trọng Điểm 0,5 đ 0,5 đ 1,0 đ Tỷ lệ 5% 5% 10% Phân Vận Chủ đề 3 biệt dụng giải Phân bĩn phân bài tốn PHỊNG GD&ĐT HUYỆN ČƯM’GAR ĐỀ KIỂM TRA I TIẾT HỌC KÌ 1 (Lần 2) TRƯỜNG THCS NGƠ QUYỀN NĂM HỌC 2017 - 2018 Mơn: Hĩa 9 ĐỀ CHÍNH THỨC Thời gian: 45 phút (khơng kể thời gian giao đề) Đề thi gồm 01 trang I. TRẮC NGHIỆM: (3 điểm) Khoanh trịn vào đáp án mà em cho là đúng. Câu 1: Thành phần % của nguyên tố dinh dưỡng nitơ cĩ trong phân bĩn KNO3 là: A.38,62%. B.13,86%. C.17,61%. D.38,61%. Câu 2: Dãy chất bazơ đều bị phân hủy ở nhiệt độ cao là: A. KOH, Mg(OH)2. B. NaOH, Al(OH)3. C. Fe(OH)3, Mg(OH)2. D. Ba(OH)2, Fe(OH)2. Câu 3: Phản ứng của cặp chất nào sau đây tạo kết tủa màu xanh: A. H2SO4 và BaCl2 B. NaOH và CuSO4 C. KOH và CaCl2 D. Ca(OH)2 và HCl Câu 4: Trong các loại phân bĩn hĩa học sau, phân bĩn kép là: A. KNO3. B. KCl. C. K2SO4. D. A và C. Câu 5: Dãy chất nào được sắp xếp theo thứ tự : oxit, axit, bazơ, muối: A. KOH, HCl, MgCl2, CuO B. MgCl2, KOH, HCl, CuO B. CuO, HCl, KOH, MgCl2 D. HCl , CuO, KOH, MgCl2 Câu 6: Nhỏ dung dịch bạc nitrat vào ống nghiệm đựng dung dịch kali clorua.Hiện tượng quan sát được là: A. Xuất hiện dung dịch khơng màu. C. Xuất hiện dung dịch màu xanh. B. Xuất hiện kết tủa màu đỏ nâu. D. Xuất hiện kết tủa trắng. II. TỰ LUẬN: (7,0 điểm) Câu 1: (2,0 điểm) Hồn thành chuỗi biến hĩa sau: ( ghi rõ điều kiện phản ứng nếu cĩ) (1) (2) (3) (4) FeCl3 Fe(OH)3 Fe2O3 Fe2(SO4)3 Fe Câu 2: (2,0 điểm) Hồn thành các phương trình hĩa học sau: t0 a) BaCl2 + H2SO4 --- b) Al(OH)3 -- — c) MgCl2 + AgNO3--- d) Zn + Pb(NO3)2 --- Câu 3: (3,0 điểm) Trộn một dung dịch cĩ hịa tan 8 gam NaOH với một dung dịch cĩ hịa tan 0,3 mol MgCl 2, thu được dung dịch A và kết tủa B. Lọc kết tủa B đem nung đến khối lượng khơng đổi thu được chất rắn C. a) Viết các phương trình hĩa học. b) Tính khối lượng C ? c) Tính khối lượng các chất cĩ trong dung dịch A ? ( Biết Mg = 24; O = 16; H = 1; Cl = 35,5 ; K = 39; Na = 23; N = 14) 1 1 Từ (1) và (2) ta cĩ: n = n = n = . 0,2 = 0,1 (mol) MgO Mg (OH )2 NaOH 2 2 0,25 điểm Khối lượng của C là: C = m = 0,1 . 40 = 4 (g) MgO 0,25 điểm c) Các chất cĩ trong dung dịch A là NaCl và MgCl2 dư. 1 1 Theo PT(1) ta cĩ: n = n = .0,2 = 0,1(mol) 0,25 điểm MgCl2 2 NaOH 2 n MgCl dư = ( 0,3 – 0,1) = 0,2 (mol) 2 0,25 điểm Khối lượng MgCl dư là : m dư = 0,2 . 95 = 19(g) 2 MgCl2 n NaCl = n NaOH = 0,2 (mol) 0,25 điểm Khối lượng NaCl là: m NaCl = 0,2 . 58,5 = 11,7 (g) (0,25 đ) ..........
File đính kèm:
 de_kiem_tra_1_tiet_hoc_ki_i_mon_hoa_hoc_lop_9_truong_thcs_ng.doc
de_kiem_tra_1_tiet_hoc_ki_i_mon_hoa_hoc_lop_9_truong_thcs_ng.doc

