Đề kiểm tra 1 tiết học kì II môn Hóa học Lớp 9 - Trường THCS Ngô Quyền - Năm học 2017-2018 - Lần 2 (Có đáp án)
Bạn đang xem tài liệu "Đề kiểm tra 1 tiết học kì II môn Hóa học Lớp 9 - Trường THCS Ngô Quyền - Năm học 2017-2018 - Lần 2 (Có đáp án)", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Đề kiểm tra 1 tiết học kì II môn Hóa học Lớp 9 - Trường THCS Ngô Quyền - Năm học 2017-2018 - Lần 2 (Có đáp án)
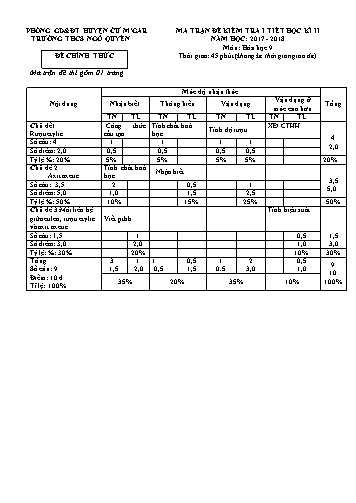
PHềNG GD&ĐT HUYỆN ČƯ M’GAR MA TRẬN ĐỀ KIỂM TRA I TIẾT HỌC Kè II TRƯỜNG THCS NGễ QUYỀN NĂM HỌC: 2017 - 2018 Mụn: Húa học 9 ĐỀ CHÍNH THỨC Thời gian: 45 phỳt (khụng kể thời gian giao đề) Ma trận đề thi gồm 01 trang Mức độ nhận thức Vận dụng ở Nội dung Nhận biết Thụng hiểu Vận dụng Tổng mức cao hơn TN TL TN TL TN TL TN TL Chủ đề1 .Cụng thức Tớnh chất hoỏ XĐ CTHH Tớnh độ rượu Rượu etylic cấu tạo học 4 Số cõu: 4 1 1 1 1 2,0 Số điểm: 2,0 0,5 0,5 0,5 0,5 Tỷ lệ %: 20% 5% 5% 5% 5% 20% Chủ đề 2 Tớnh chất hoỏ . Nhận biết Axit axetic học 3,5 Số cõu: 3,5 2 0,5 1 5,0 Số điểm: 5,0 1,0 1,5 2,5 Tỷ lệ %: 50% 10% 15% 25% 50% Chủ đề 3:Mối liờn hệ Tớnh hiệu suất giữa etilen, rượu etylic Viết pthh và axit axetic Số cõu: 1,5 1 0,5 1,5 Số điểm: 3,0 2,0 1,0 3,0 Tỷ lệ: %: 30% 20% 10% 30% Tổng 3 1 1 0,5 1 2 0,5 9 Số cõu: 9 1,5 2,0 0,5 1,5 0.5 3,0 1,0 10 Điểm: 10 đ 35% 20% 35% 10% 100% Tỉ lệ: 100% PHềNG GD&ĐT HUYỆN ČƯ M’GAR HƯỚNG DẪN CHẤM ĐỀ KIỂM TRA I TIấT TRƯỜNG THCS NGễ QUYỀN NĂM HỌC: 2017 - 2018 Mụn: Húa học 9 ĐỀ CHÍNH THỨC Thời gian: 45 phỳt (khụng kể thời gian giao đề) Đỏp ỏn đề thi gồm 01 trang I. Trắc nghiệm (3,0 điểm) Mỗi đỏp ỏn đỳng được 0, 5 điểm Cõu 1 2 3 4 5 6 Đỏp ỏn c b a d b a Cõu Nội dung Điểm xt 1. 2C2H10 + 5O2 t0 4CH3COOH + 2H2O 0,5 điểm 0 1 H2SO4 ,t 2.CH COOH + C H OH CH COOC H + H O (2,0 3 2 5 3 2 5 2 0,5 điểm t0 điểm 3.CH3COOC2H5+ NaOH CH3COONa + C2H5OH 0 ) t 0,5 điểm Hoặc: CH3COOC2H5 + H2O xt C2H5OH + CH3COOH 4. 2C H OH + 2Na 2C H ONa + H 2 5 2 5 2 0,5 điểm * Gồm 2 tớnh chất. 2 1. Tỏc dụng với nước Glixerol + Cỏc axit bộo. t0 0,75 điểm (2,0 PTHH: (RCOO)3C3H5 + 3H2O axit C3H5(OH)3 + 3RCOOH điểm 2. Tỏc dụng với kiền Glixerol + Muối của cỏc axit bộo. 0 0,75 điểm ) PTHH: (RCOO) C H + 3NaOH t C H (OH) + 3RCOONa 3 3 5 3 5 3 0,5 điểm * CTTQ: (R – COO)3C3H5 t0 a)PTHH : C2H5OH + 3O2 2CO2 + 3H2O (1) 0,5 điểm 11,2 1 1 b)n = 0,5(mol) . Theo pt n n .0,5 0,25(mol) CO2 22,4 C2H5OH 2 CO2 2 0,25 điểm Khối lượng của C H OH tạo thành là : m = 0,25 .46 = 11,5(g ) 2 5 C2H5OH 3 3 0,25 điểm c)Theo pt: n n .0,5 0,75(mol) O2 2 CO2 2 0,25 điểm 0,25 điểm Thể tớch của O2 tham gia pư là : V = 0,75 . 22,4 = 16,8 (lit ) O2 0,25 điểm 16,8.100 Thể tớch của khụng khớ cần dựng cho pư trờn là : Vkk = 84(lit) 0,25 điểm 3 20 m 6,4 (3,0 d) n = O2 = 0,2 (mol) 0,25 điểm O2 điểm M O 32 mengiam ) PTHH : C2H5OH + O2 CH3COOH + H2O (2 ) Theo PT: 1mol 1 mol Theo đb: 0,1 mol 0,2 mol 0,25 điểm 0,1 0,2 Lập tỷ lệ : mol < n dư tớnh theo n 1 1 O2 C2H5OH Theo pt(2) ta cú n = n = 0,1 (mol) CH3COOH C2H5OH 0,25 điểm Khối lượng của CH COOH là : m = 0,1 . 60 = 6 (g) 3 CH3COOH mtt 4,5.100% Hiệu xuất phản ứng là : H = .100% 75% 0,25 (0,25 điểm ủ) ......... mlt 6
File đính kèm:
 de_kiem_tra_1_tiet_hoc_ki_ii_mon_hoa_hoc_lop_9_truong_thcs_n.doc
de_kiem_tra_1_tiet_hoc_ki_ii_mon_hoa_hoc_lop_9_truong_thcs_n.doc

